Хирургическое лечение перфоративных пилородуоденальных язв вчера и сегодня
Актуальность проблемы
Язвенная болезнь желудка и двенадцатиперстной кишки (ДПК) является одним из самых распространенных заболеваний, поражая 2–10% населения экономически развитых стран [Druart M. L., 1997; Ивашкин В. Т., 2001; Кузин М. И., 2002; Phillipo L., 2011; Michal Ž., 2014]. В настоящее время в лечении язвенной болезни с успехом применяется медикаментозная терапия. Достижения конца XX столетия внесли радикальные изменения в понимание патогенеза язвенной болезни и ее течение, что способствовало совершенствованию комплексной терапии с применением мощных антисекреторных и антибактериальных препаратов. Современные схемы лечения позволяют добиться эрадикации Hp более чем в 90% случаев, что приводит не только к ускорению сроков рубцевания язвы, но и к многократному снижению числа рецидивов. Широкое внедрение мощных антисекреторных препаратов и их бесконтрольное применение привело к значительному уменьшению в последние годы количества плановых операций по поводу язвенной болезни, но при этом появилась тенденция к явному росту числа пациентов с осложненным течением этого заболевания, нуждающихся в оперативном лечении [Бабкин О.В., 2003]. Такое осложнение, как перфорация язвы (ПЯ) представляет реальную угрозу для жизни пациента. Летальность при ПЯ остается высокой и составляет 5–15% [Курыгин А. А., 2001; Борисов А. П., 2003; Phillipo L., 2011; Michal Ž., 2014]. На долю перфоративных пилородуоденальных язв приходится 0,1% среди хирургических заболеваний, а в структуре ургентной абдоминальной хирургической патологии 1,9–2,6% [Сацукевич В. Н., 2001; Michal Ž., 2014]. Пилорические и препилорические язвы (желудочные язвы III типа по
Первым хирургическим вмешательством по поводу ПЯ было ее ушивание, по праву считающееся первой органосохраняющей операцией. После того, как в 1880 году Johan Mikulicz выполнил ушивание травматической перфорации желудка, подобные операции выполняли Czerny (1885 г.), Taylor (1887 г.), Dean (1888 г.), Wahl (1890 г.). В России первое успешное ушивание ПЯ (УПЯ) ДПК выполнено
Однако УПЯ в условиях
В последние годы широкое внедрение малоинвазивных и видеолапапроскопических оперативных вмешательств привлекло дополнительное внимание к ушиванию ПЯ. Впервые лапароскопическое закрытие перфоративного отверстия луковицы ДПК прядью большого сальника и фибриновой пломбой выполнил в 1989 году P. Mouret [Br. J. Surg., 1990]. В 1990 году
Однако при всех преимуществах УПЯ является паллиативной операций, не влияющей на звенья патогенеза язвенной болезни и по данным разных авторов сопровождающейся развитием рецидива заболевания у 80% больных. Еще
Совершенствуя технику оперативного лечения ПЯ ряд хирургов предложили не ушивать, а иссекать ПЯ. В случаях локализации язвы вблизи привратника с целью избежания в последующем стеноза выходного отдела желудка (ВОЖ) и гастростаза они выполняли расширение пилорического канала путем поперечного рассечения привратника. Эти операции получили название пилоропластики (ПП). В 1915 году S. Judd и Horsley выполнили ромбовидное иссечение небольших ПЯ ДПК с рассечением привратника. В 1963 году Tanaka предложил модификацию этой операции, выполняя переднюю гемипилорэктомию.
По мнению ряда авторов, одна только ПП снижает желудочную секрецию не менее чем на 17–18% [Майстренко Н. А., 2000; Панцырев Ю. М., 1978].
Одним из преимуществ ПП является возможность выполнения интрадуоденальной ревизии для выявления «зеркальной» язвы, что невозможно при выполнении УПЯ [Тищенко А. М., 1995]. Ряд авторов [Курыгин А. А., 1992] отмечают, что в 5–7% случаев ПЯ передней стенки луковицы ДПК сочетается с кровотечением и иссечение краев язвенного дефекта полностью исключает возможность оставления кровоточащего сосуда в нем.
Накопленный клинический опыт выполнения дренирующих желудок операций показывает, что они могут вызывать целый ряд патологических синдромов. В 1970 году Johnston [Br. J. Surg., 1970] и Hedenstedt [Copenhagen, 1970], оценивая причины неудовлетворительных результатов органосохраняющих операций при язвенной болезни, увидели их в разрушении привратника. G. Grassi [Brit. J. Surg., 1971],
К недостаткам дренирующих операций относят деформацию пилородуоденальной зоны с формированием дивертикулоподобных карманов. В позднем послеоперационном периоде это приводит к пролонгированию гормональной фазы желудочной секреции и рецидиву язвы [
В 1978 году Helwing E., Heymann H. [Chirurg, 1978], Grassi G. [Brit. J. Surg, 1971] выполнили циркулярную постпилорическую резекцию ДПК в пределах верхнего и нижнего краев язвы без мобилизации обоих отрезков кишки. При этом заднюю стенку проксимального отдела ДПК они подшивали к язвенному краю ее дистального отдела. Швы накладывались через патологические ткани и края язвы, тем самым снижая качество операции.
Принципам нового направления в функциональной хирургической гастроэнтерологии полностью соответствует разработанный
Одновременно с органосохраняющими операциями на желудке развивалось и радикальное направление в лечении язвенной болезни желудка и ДПК. В отечественной хирургии наиболее активным пропагандистом резекции желудка (РЖ) в лечении язвенной болезни был
- наличие язвенного анамнеза до прободения (в особенности при наличии в анамнезе кровотечения или перфорации);
- сроки от перфорации до операции не превышают 6–8 часов;
- удовлетворительное общее состояние больного при отсутствии сопутствующих заболеваний;
-
отсутствие в брюшной полости гнойного экссудата и большого количества
желудочно-дуоденального содержимого; - возраст больного от 25 до 50 лет;
- наличие подготовленных хирургов высокой квалификации.
Большинство хирургов
В ряде случаев РЖ становится самостоятельной болезнью вследствие развития пострезекционных синдромов. По этому поводу существуют разнообразные теории: механическая, химическая, электролитическая, нейрогуморальная,
Процент нетрудоспособности после РЖ по результатам исследований
Помимо резекции 2/3 желудка в арсенале хирурга имеется более щадящий метод лечения — так называемая экономная резекция, именуемая в литературе антрумэктомией, часто сочетаемая с ваготомией. На заре внедрения ваготомии с антрумэктомией в хирургическую практику рекомендовалось удалять 10% желудка [Scott H. W., 1966], затем объем РЖ был расширен до 20–30%, а в последующем большинство хирургов под антрумэктомией стали понимать удаление 40–60% желудка. Столь противоречивые данные обусловлены тем, что антральный отдел, как гастринпродуцирующая часть желудка, занимает различную по протяженности часть этого органа у разных людей — от 10 до 80% [Ruding R., 1963]. Твердо установлено, что после ваготомии с антрумэктомией у 60% больных развивается ахлоргидрия вплоть до гистаминорезистентной и еще у 30 — 35% продукция свободной соляной кислоты находится на таком уровне, при котором развитие пептической язвы маловероятно. Рецидив язвы после этой операции наблюдается от 0,6% до 4,5% [Goligher J. C., 1972]. Курыгин А. А. с соавт. [СПб.: Гиппократ, 1992.] считает, что антрумэктомия в комбинации с ваготомией наиболее выгодна из всех существующих методов хирургического лечения язвы ДПК у больных с крайне активной секреторной функцией желудка (при отсутствии гастриномы), а также у некоторых больных при рецидиве заболевания после ваготомии с дренирующей желудок операцией.
В последние годы все чаще появляются сообщения об эндоскопических резекциях желудка с последующей реконструкцией
С разработкой и внедрением в клиническую практику ваготомии при язвенной болезни появились попытки использовать ее и при осложнениях. В 1953 году Jelinek первым применил стволовую ваготомию при ушивании ПЯ ДПК. Ее ценность видели в возможности влиять на патогенетические механизмы язвенной болезни, секрецию, моторику желудка и добиваться не только спасения жизни больного, но и его полного излечения. В 1969 году в России впервые
Однако стволовая ваготомия, занимая меньше времени и будучи более простой в техническом исполнении, сопровождается большим числом постваготомических осложнений. Устранение первой фазы секреции приводит к усилению второй фазы вследствие длительной задержки пищевых масс в желудке с последующим возникновением стазовых язв. Также иннервации лишаются печень, желчные пути, поджелудочная железа, тонкая и большая часть толстой кишки, происходит денервация привратника и антрального отдела желудка. По данным разных авторов, после стволовой ваготомии демпинг синдром наблюдался в 5–20% случаев, диарея — 10–30%, развитие холестаза и холелитиаза в 0,8–1,7% случаев [Панцырев, 1979].
В настоящее время вопросы эффективности ваготомии и выбора ее способа, особенно в ургентной хирургии, остаются предметом оживленной дискуссии хирургов всего мира. В современной литературе эти вопросы освещены недостаточно и носят противоречивый характер. Разработан целый ряд модификаций ваготомий [Taylor T.
Неоднозначность тактических подходов в хирургическом лечении осложненной язвенной болезни побуждает к изучению не только непосредственных, но и отдаленных результатов каждого метода операции. Поиск наиболее рациональной и эффективной методики хирургического лечения перфоративных пилорических и препилорических язв (ПППЯ) в эпоху новых возможностей противоязвенной терапии является весьма актуальной проблемой ургентной хирургии.
Цель работы
Улучшение ближайших и отдаленных результатов хирургического лечения больных с перфоративными пилорическими и препилорическими язвами.
Материалы и методы исследования
Изучены непосредственные результаты хирургического лечения 253 пациентов с перфоративными пилорическими язвами (с января 2003 года по февраль 2012 года. Ретроспективному анализу (
Проспективному анализу (
Среди пациентов было 205 мужчин и 48 женщин, возраст больных колебался от 16 до 95 лет, составляя в среднем 39,8 ± 18 лет.
Все пациенты разделены на три группы в зависимости от вида оперативного вмешательства:
I группа — пациенты, которым выполнено УПЯ (
Абсолютными показаниями к ушиванию ПЯ считали небольшие размеры дефекта (до 1,5 см) при отсутствии каллезных краев; возраст больного (до 60 лет), при отсутствии длительного язвенного анамнеза; срок не более 12 часов с момента перфорации при наличии распространенного гнойного перитонита.
II группа — пациенты, которым были выполнены различные варианты дренирующих желудок операций (
Абсолютными показаниями к иссечению язвы с последующей ПП считали наличие длительного язвенного анамнеза; наличие периульцерозных рубцовых изменений; большой язвенный инфильтрат (более 1,5–2 см).
III группа — пациенты, которым выполнена РЖ по Бильрот II в. модификации
РЖ выполнялась при перфорации хронических язв с длительным анамнезом, резистентных к консервативному лечению; при неоднократных перфорациях в анамнезе или перенесенных эпизодах кровотечения, неудалимых больших пенетрирующих язвах; в ситуациях, когда нельзя было исключить перфорацию опухоли желудка с локализацией в выходном отделе.
Критерии включения в исследование для органосохраняющих операций:
1) наличие изолированного осложнения в виде перфорации хронической язвы;
2) локализация язвенного субстрата в пилорическом и препилорическом отделе желудка;
3) тяжесть состояния в пределах 3–4 по шкале ASA;
4) местные условия, исключающие необходимость резекционного метода вмешательства и оставляющие возможность выбора между ушиванием и иссечением ПЯ с ПП.
Отдаленные результаты лечения прослежены у 121 пациента: 54 пациента I группы (ушивания ПППЯ) и 58 пациентов II группы (иссечение с различными видами ПП). Все они были вызваны на амбулаторное обследование, в ходе которого произведена оценка качества их жизни в процессе анкетирования по шкале MOS
Собственные результаты исследования
После ВЛС операций у 18 пациентов парез кишечника не отмечен. В первые сутки стали отходить газы, на 2–3 сутки был самостоятельный стул. У семи пациентов парез кишечника разрешился на вторые сутки. У одного пациента развилась несостоятельность швов ушитой ПЯ. После традиционных лапаротомных ушиваний послеоперационный парез разрешался на 2–3 сутки после операции, что характеризовалось светлым желудочным отделяемым по назогастральному зонду. У одного пациента развилась ранняя спаечная кишечная непроходимость. После ПП послеоперационный парез разрешался чуть раньше — на вторые сутки после операции. Восстановление
В 1–2 сутки практически все пациенты, перенесшие ВЛС вмешательство, были активизированы и основной жалобой были боли в области стояния дренажной трубки, исчезнувшие сразу после ее удаления. Срок активизации этих пациентов был достоверно меньше срока активизации пациентов, перенесших открытое ушивание (t = 3,6; p < 0,05) и иссечение язвы с ПП (t = 4,4; p < 0,05). Пациенты, перенесшие открытые вмешательства, были активизированы на 2–3 сутки (t= 0,9; p > 0,05). После всех операций из традиционного лапаротомного доступа болевой синдром сохранялся в течение трех суток, тогда как после ВЛС вмешательств достоверно меньше — двух суток.
При выполнении ПП в шести случаях (4,8%) мы выявили «зеркальную язву», в двух случаях с признаками состоявшегося кровотечения. Выполнено прошивание сосуда в язве задней стенки пилорического канала.
Достоверных различий по характеру температурной реакции между I и II группами пациентов не выявлено на первые сутки, а также с 3 по 7 сутки (t < 2,0; p > 0,05).
Осложнения в раннем послеоперационном периоде в I группе после ушиваний ПЯ (21 случай) и во II группе после иссечения язвы с ПП (25 случаев) возникали с одинаковой частотой (t = 0,3; p > 0,05).
Летальность в I группе составила 2,1% (2 пациента) и во II группе — 3,2% (4 пациента). Достоверных различий показателей летальности не выявлено. Основной причиной летальности послужила интоксикация на фоне распространенного перитонита, причем у одного пациента имел место вялотекущий продолжающийся послеоперационный перитонит в связи с несостоятельностью швов ушитой язвы.
В программу послеоперационного обследования мы включили рентгенографию желудка с бариевой взвесью, ЭГДС с проведением
По этой программе было обследовано 34 пациента I группы и 32 пациента II группы.
При выполнении рентгенологического исследования у пяти (14,7%) пациентов I группы выявлено наличие компенсированного и у одного (2,9%) пациента субкомпенсированного стеноза ВОЖ, главным образом после операции
При выполнении ЭГДС с
Сравнительная оценка функции ВОЖ после иссечения язвы с различными вариантами ПП свидетельствует о функциональных преимуществах этих вмешательств перед ушиванием перфоративного отверстия.
При анализе продолжительности лечения пациентов отмечено, что после иссечения ПППЯ с ПП, а также после ВЛС операций меньшее число пациентов нуждалось в госпитализации в РАО, но различия недостоверны. Средняя продолжительность
Болевой синдром у пациентов, перенесших РЖ, был более выраженным и требовал в 71,9% случаев применения наркотических анальгетиков и купировался лишь к 4–5 суткам. Активизация пациентов и начало энтерального питания при неосложненном течении после РЖ обычно наступала на 5–6 сутки. К этому сроку удаляли назогастральный зонд, заведенный за зону гастроэнтероанастомоза для декомпрессии. Противоязвенная терапия пациентам после резекции 2/3 желудка по Бильрот II в. модификации
Таблица 1. Продолжительность
| Показатель |
I группа, открытое ушивание ( |
I группа, ВЛС ушивание ( |
II группа, ПП ( |
|
Нуждающиеся в госпитализации в РАО в послеоперационном периоде |
40 (58,8%) | 12 (41,4%) | 56 (45,2%) |
|
Средняя продолжительность |
3,0 ± 4,0 | 1,6 ± 1,2 | 2,2 ± 2,5 |
|
Средняя продолжительность |
10,1 ± 5,9 | 8,1 ± 1,3 | 11,1 ± 3,4 |
После РЖ послеоперационный парез разрешался на 4–5 сутки после операции, что характеризовалось прекращением гастростаза и светлым желудочным отделяемым по назогастральному зонду.
Средняя продолжительность
Летальность после РЖ составила 21,9% (7 пациентов). Основными причинами летальных исходов явились декомпенсация сердечной недостаточности, тромбоэмболия мелких ветвей легочной артерии, нарушение мозгового кровообращения.
Отдаленные результаты лечения были прослежены у 54 пациентов I группы, которым были выполнены ушивания ПППЯ, и 58 пациентов II группы, перенесшим иссечение язв с различными видами ПП. Все они были обследованы в амбулаторном порядке. Сроки от момента операции составили от 1 года до 7 лет.
После УПЯ процент рецидивного язвообразования в разные сроки после операции составил 64,8% (35 пациентов из 54). Среди причин отмечены несоблюдение режимов противоязвенной терапии, часть пациентов не имела материальной возможности покупать дорогостоящие препараты, часть пациентов указывала на «плотный» график работы и нехватку времени на амбулаторное обследование, прием препаратов, тем более соблюдение диеты. 8 пациентов I группы из 54 (14,8%) вынуждены время от времени обращаться за врачебной помощью по поводу язвенной болезни и находятся на диспансерном учете, соблюдать строгую диету, неоднократно лечиться по поводу язвенной болезни.
Во II группе пациентов, согласно данным опроса, рецидив язвы был выявлен у 9 пациентов из 58 (15,5%), различия достоверны.
При ЭГДС у большинства пациентов I группы, 43 из 54 (79,6%) , также, как и у пациентов II группы, у 47 из 58 (81,0%) отмечается картина распространенного гастрита, достоверного различия между группами нет. У 9 из 54 (16,7%) пациентов I группы выявлен грубый постязвенный рубец, в то время как у пациентов из II группы грубой деформации привратника в зоне ПП и лигатурных компонентов выявлено не было.
У 45 (83,3%) из 54 пациентов I группы и у 41 (70,7%) из 58 пациентов II группы выявлена обсемененность Helicobacter pylori. Достоверной разницы по степени обсемененности между группами I и II не выявлено.
Анализ эвакуаторной функции желудка показал, что в отдаленном послеоперационном периоде случаев ускоренной эвакуации бария у всех обследованных пациентов отмечено не было, а вот замедленная эвакуация с признаками компенсированного стеноза желудка выявлена достоверно чаще после УПЯ 26,0% (14 из 54) против 8,6% (5 из 58) в группе пациентов после ПП, различия достоверны.
3 пациентам I группы с язвами пилорического канала (в трудоспособном возрасте 33–55 лет),
Ни один из пациентов после иссечения язвы с ПП не был госпитализирован по поводу обострения или
Отдаленные результаты РЖ прослежены у 9 пациентов, в возрасте от 31 до 58 лет, в сроки от 2 до 6 лет после операции. Всем обследуемым выполнена ЭГДС для оценки морфофункционального состояния культи желудка.
В процессе телефонного анкетирования удалось установить (со слов родственников), что смерть двух пациентов наступила от осложнений язвенной болезни.
Качество жизни в отдаленные сроки (от 1 до 7 лет) изучено у 54 (55,7%) пациентов I группы и у 58 (46,8%) пациентов II группы. Средний срок анкетирования после УПЯ составил 3,5 ± 1,7 лет, после иссечения язвы с ПП — 3,7 ± 1,6 лет, группы сопоставимы. В контрольную группу вошли 35 здоровых людей из числа сотрудников стационара.
При анализе средних показателей шкал опросника качества жизни MOS
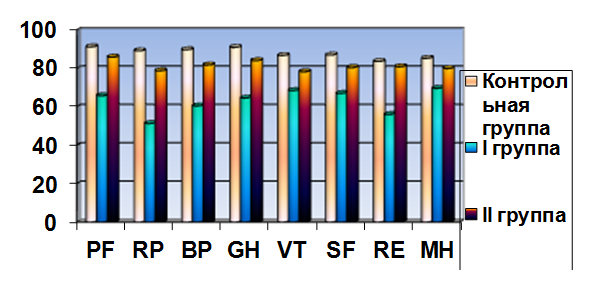
Рисунок 1. Распределение показателей шкал опросника MOS
|
|
PF |
RP |
BP |
GH |
VT |
SF |
RE |
MH |
|
Контрольная группа |
91,4 |
89,3 |
89,9 |
91,1 |
86,9 |
87,1 |
83,8 |
85,4 |
|
I группа |
65,9 |
51,4 |
60,6 |
64,7 |
68,6 |
67,1 |
56,1 |
69,8 |
|
II группа |
86 |
78,9 |
81,9 |
84,2 |
78,4 |
80,6 |
81 |
80,1 |
Показатели физического компонента здоровья (PH) и психического компонента здоровья (MH) также достоверно выше у пациентов, перенесших иссечение ПППЯ с различными видами ПП (t = 6,9, p < 0,05 и t = 4,4, p < 0,05 соответственно).
Полученные результаты свидетельствуют о более высоком качестве жизни пациентов после различных вариантов ПП.
Показатели качества жизни пациентов после РЖ были ниже показателей I и II групп, в целом пациенты оставались трудоспособными и не нуждались в медицинской помощи.
Выводы
1. Непосредственные результаты открытых органосохраняющих операций (ушивание и иссечение с различными вариантами ПП) принципиально не отличаются по количеству осложнений и течению послеоперационного периода: продолжительности пареза кишечника, срокам активизации пациентов, длительности болевого синдрома, характеру температурной реакции, необходимости в госпитализации и средней продолжительности пребывания в РАО.
2. Непосредственные результаты ВЛС ушивания ПППЯ имеют преимущество в уменьшении болевого синдрома, длительности пареза кишечника, сроков активизации пациентов, средней продолжительности
3. РЖ в ближайшем послеоперационном периоде характеризуется длительным периодом реабилитации, увеличением числа послеоперационных осложнений (62,5%) и летальности (21,9%).
4. Отдаленные результаты комбинации ушивания ПППЯ по сравнению с иссечением язвенного субстрата с ПП и эрадикационной противоязвенной терапией с учетом комплаентности больного характеризуются большей частотой рецидивного язвообразования (до 64,8%) и стенозированием ВОЖ (до 16,7%), (рецидив выявлен у 15,5%, стенозирования не отмечено).
5. Качество жизни пациентов по шкале MOS
Литература
Нечипоренко Е. И., Черепанин А. И., Антонов О. Н, Рыбальченко
Дземешкевич С. Л., Черепанин А. И., Антонов О. Н, Рыбальченко
Антонов О. Н, Рыбальченко
Черепанин А. И., Покровский К. А., Антонов О. Н, Рыбальченко А. В., Шеров
Черепанин А. И., Антонов О. Н., Негребов М. Г., Баулина Е. А., Рыбальченко

