Хронический гастрит, ассоциированный с Helicobacter pylori: современные стандарты диагностики и новые возможности эндоскопии
Хронический гастрит является наиболее распространенным заболеванием и занимает одно из первых мест в структуре заболеваний
Helicobacter pylori (Н.pylori) — грамотрицательная микроаэрофильная бактерия, колонизирующая слизистую оболочку желудка и ассоциированная с атрофическим гастритом, язвенной болезнью желудка и двенадцатиперстной кишки, аденокарциномой и экстранодальной
Новые европейские рекомендации по инфекции H.pylori, представленные на очередном XXIV заседании Международной рабочей группы по изучению Helicobacter pylori и родственным бактериям при хронических воспалительных процессах пищеварительного тракта и раке желудка (XXIVth International Workshop on Helicobacter and related bacteria in chronic digestive inflammation and gastric cancer) 11–13 cентября 2011 года, были посвящены не только новым подходам к терапии, но и современным методам диагностики инфекции Н.pylori. Эти методы делятся на инвазивные и неинвазивные. Все инвазивные методы диагностики предусматривают проведение эндоскопического исследования с забором биопсийного материала — биоптатов слизистой оболочки желудка. Эндоскопическое исследование является одним из самых важных методов оценки слизистой оболочки желудка у пациентов с H.pylori ассоциированной патологией. Применение узкоспектральной эндоскопии в комбинации с оптическим увеличением изображения позволяет дифференцировать патологические изменения, которые при обычной эндоскопии не могут быть выявлены. Неинвазивные методы — это различного рода иммунологические исследования, позволяющие определять наличие антител в сыворотке крови или бактериального антигена Н.pylori в фекалиях, ПЦР исследование с определением ДНК Н.pylori в фекалиях и уреазный дыхательный тест с С13 или С14 меченным атомом углерода.
История открытия Helicobacter pylori
Впервые идея об инфекционном развитии гастрита возникла в конце ХХ века, когда в желудке животных были найдены спиралевидные бактерии. В 1893 году G. Bizzozero выявил спиралевидные бактерии в париетальных клетках желудка собак. В 1896 году H. Salomon установил, что эти бактерии могут передаваться от зараженных мышей кошкам и собакам. Первые описания спиралевидных бактерий в желудке человека принадлежат W. Krienitz (1906) и A. Luger (1917), которые обнаружили их на изъязвившейся карциноме желудка. Дальнейшие исследования проводились на операционном и биопсийном материалах. L. Barron обнаружили «спирохеты» в 37% случаев в желудках, резецированных по поводу язвенной болезни и карциномы. В 1940–1954 годах S. Freedberg и
Таблица 1. Распространенность инфекции H.pylori и смертность от рака желудка в странах с различным
| Страна |
Инфицированность H. pylori, % | Смертность (рак желудка) |
|
Китай Россия и Япония |
80-100 60-80 |
Более 30 человек на 100 000 населения |
|
Алжир Коста-Рика Кот-Дивуар Нигерия Чили Эквадор |
75-95 | Более 30 человек на 100 000 населения |
|
Австралия Бельгия Великобритания Израиль Канада Новая Зеландия США Франция |
4 5 9 15 13,6 5 23 20 |
Менее 10 человек на 100 000 населения |
Приведенные данные свидетельствуют о более высокой заболеваемости раком желудка в тех регионах, где выше показатели заболеваемости H.pylori ассоциированным гастритом.
Современные методы лабораторной диагностики инфекции Helicobacter pylori
С момента открытия Н.pylori прошло чуть более тридцати лет. За этот период времени было разработано большое количество методов лабораторной диагностики, позволяющих выявлять и идентифицировать этот микроорганизм. Однако в настоящее время ни один из существующих методов лабораторной диагностики инфекции Н.pylori не универсален. Пределы возможностей этих методов могут быть ограничены не только их чувствительностью, но, зачастую, зависят от возраста пациента, его индивидуальных особенностей, стадии заболевания, а также индивидуальных особенностей течения инфекции. Все существующие на сегодняшний день методы лабораторной диагностики инфекции Н.pylori делятся на две большие группы: инвазивные и неинвазивные методы (табл. 2).
Таблица 2. Методы лабораторной диагностики инфекции Н.pylori
| Инвазивные методы | Неинвазивные методы |
| Бактериологический метод
Гистологический метод Молекулярно-биологический метод (ПЦР) Фазово-контрастная микроскопия Быстрый Уреазный тест |
Серологический метод Молекулярно-биологический метод (ПЦР) Уреазный дыхательный тест |
Принципиальное значение для практики имеет проведение диагностики Н.pylori инфекции до лечения (первичная диагностика), и после проведения противохеликобактерной терапии (контроль эффективности выбранной схемы лечения). Первичная диагностика Н.pylori инфекции должна осуществляться методами, непосредственно выявляющими бактерию или продукты ее жизнедеятельности в организме больного. Таким требованиям удовлетворяют следующие методы диагностики:
1. Бактериологический метод — посев биоптата слизистой оболочки желудка или двенадцатиперстной кишки на
2. Дыхательный тест — определение в выдыхаемом больным воздухе изотопов С13 или С14, которые выделяются в результате расщепления в желудке больного меченой мочевины под действием фермента уреазы Н.pylori.
3. Быстрый Уреазный тест — определение уреазной активности в биоптате слизистой оболочки желудка или двенадцатиперстной кишки путем помещения его в жидкую или гелеобразную среду, содержащую субстрат, буфер и индикатор.
4. Гистологический метод — золотой стандарт диагностики Н.pylori инфекции и хронического гастрита.
Бактериологический метод является единственным методом исследования, обладающим 100% специфичностью. Он позволяет выделить чистую культуру Н.pylori, провести ее идентификацию, изучить морфологические, биохимические и биологические свойства бактерий. В эпидемиологической практике выделение чистой культуры Н.pylori необходимо для внутривидового типирования штаммов, что может быть использовано при мониторинге для дифференциации между реинфекцией новым штаммом и рецидивированием инфекции, которое может быть обусловлено тем же штаммом. В научной практике бактериологический метод важен, так как позволяет изучать факторы патогенности Н.pylori и изготовлять препараты для серологической диагностики. Как и любой метод диагностики, бактериологический метод исследования обладает не только достоинствами, но и недостатками, которые зачастую ограничивают его широкое использование в клинической практике. К недостаткам этого метода относятся, прежде всего, необходимость специального лабораторного оборудования, реактивов, специальных питательных сред, а также обученных специалистов. Все это сопряжено с большими материальными затратами. Результаты бактериологического исследования отсрочены от момента взятия биопсийного материала минимум на 3–5 дней, а при необходимости получения данных о чувствительности Н.pylori к антибактериальным препаратам длительность исследования увеличивается и составляет в среднем 6–7 дней. Кроме того, для проведения бактериологического исследования необходимо проведение эзофагогастродуоденоскопии с забором биопсийного материала.
Уреазный дыхательный тест (УДТ) основан на способности уреазы разлагать мочевину до НСО3I и NH4+. Из НСО3I образуется СО2, который попадая в кровоток затем транспортируется в легкие. Для проведения УДТ необходима мочевина, меченная радиоактивным углеродом 13С или 14С. Чаще в клинической практике используется нерадиоактивный стабильный углерод 13С. 14С используется реже, так как является источником излучения низкоэнергетических β-частиц, которые обнаруживаются сцинтиляционным счетчиком. Изотоп количественно определяют газовым спектрометром. В начале исследования берутся две фоновые пробы выдыхаемого воздуха. Далее пациент съедает легкий завтрак и тестовый субстрат и в течение одного часа, с интервалом в 15 минут у него берут по четыре пробы выдыхаемого воздуха. Уровень радиоактивного изотопа в выдыхаемом воздухе определяется в течение 10–30 минут. Затем пробирки направляются на
Быстрый урезаный тест основан на определении в биоптате слизистой оболочки желудка местной уреазной активности H.pylori. Быстрота изменения окраски индикатора (с желтого цвета на красный или малиновый) зависит от уреазной активности, которая в свою очередь зависит от количества бактерий. К недостаткам теста относится его инвазивность, невозможность морфологической оценки состояния слизистой оболочки желудка, а также получение ложноотрицательных (при малом количестве микробных тел) или ложноположительных результатов (контаминирование материала другими уреазопродуцентами, например H.heilmannii —
Гистологический метод — золотой стандарт диагностики инфекции H.pylori, который является наиболее объективным методом, так как позволяет обнаружить возбудитель инфекции, определить положение бактериальных тел в слизи, покрывающей слизистую оболочку желудка, наблюдать взаимоотношение Н.pylori с апикальной мембраной эпителиоцитов, а также определить пути взаимодействия бактерии с тканями макроорганизма (рис. 2). Забор биопсийного материала производится из зон слизистой оболочки желудка с признаками наиболее активного воспалительного процесса (максимально выраженная гиперемия и отeк). Биопсия и забор материала для диагностики инфекции из области дна язв и эрозий, а также из их краев, является ошибкой, так как в них нет эпителиальных клеток, обладающих свойствами, необходимыми для адгезии и колонизации Н.pylori. Поскольку бактерии Н.pylori могут быть распределены неравномерно в различных отделах желудка, для повышения чувствительности метода, а также для оценки состояния слизистой оболочки и определения типа и локализации гастрита, степени его выраженности биоптаты целесообразно брать из антрального, фундального отделов, а также области угла желудка (рис. 1).
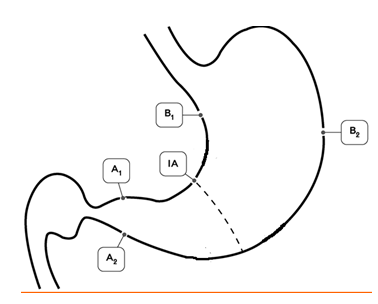
Рисунок 1. Схема выполнения биопсии слизистой оболочки желудка с целью достоверной диагностики инфекции H.Pylori и гастрита в пяти зонах желудка: две биопсии — в антральном отделе (А1 и А2), две биопсии — в теле желудка (В1 и В2) и одна биопсия в зоне угла желудка (IА).

Рисунок 2. Диагностика инфекции Н.pylori при окраске гистологического препарата красителем акридиновым оранжевым, бактерии определяются в виде мелких, слегка извитых палочек, находящихся в слое слизи над поверхностью эпителия желудка в непосредственной близости от слизистой оболочки желудка и на поверхности эпителиальных клеток.
Классификация количественной и качественной оценки инфекции H. pylori, степени воспаления при гастрите, атрофии и кишечной метаплазии была предложена в Сиднейской системе и ее Хьюстонской модификации, однако эта система не позволяла оценивать прогноз повреждения. Современная классификация и оценка степени и стадии гастрита OLGA (Operative Link for Gastritis Assessment) основана на оценке стадийности и степени выраженности атрофического гастрита в фундальном и антральном отделах желудка [13, 14]. Под степенью гастрита понимается выраженность суммарной воспалительной инфильтрации (нейтрофильными лейкоцитами и мононуклеарными клетками), под стадией — выраженность атрофии. Чем выше выраженность атрофии и больше объем поражения слизистой оболочки желудка, тем выше риск развития неоплазии. Таким образом, новая система определения стадии гастрита OLGA обеспечивает определение прогноза развития предраковых изменений, позволяет клиницисту получить представление о распространенности повреждения слизистой оболочки желудка и степени риска развития рака желудка [15, 16].
Цитологический метод применяется преимущественно в России. Метод основан на выявлении бактериальных тел в
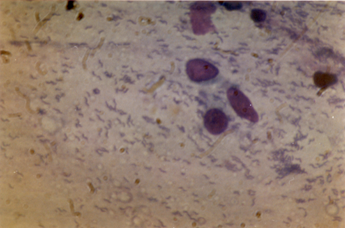
Рисунок 3. Цитологическая диагностика H.pylori инфекции: множественные бактерии спиралевидной формы определяются в
В последние годы в клинической практике начал использоваться серологический скрининг заболеваний желудка, включающий определение в сыворотке крови антител класса G к H.pylori (
Генотипирование Helicobacter pylori
Несмотря на высокий процент инфицирования населения H.pylori, подавляющее большинство инфицированных лиц не имеют клинических проявлений на момент диагностики, но они, тем не менее, представляют собой группу риска, в которой с течением времени развивается хронический гастрит, может развиться язвенная болезнь, предраковые изменения слизистой оболочки, а также аденокарцинома желудка. К настоящему времени у двух штаммов H.pylori (J99 и 26695) определены полные последовательности генома. Геном H.pylori содержит ¬ 1600 генов [19]. Ряд генов, продуктами которых являются белки CagA, VacA, IceA, BabA, считаются факторами патогенности. Ген cagA (
Новые эндоскопические технологии диагностики хронического гастрита, ассоциированного с H.pylori
Эндоскопическое исследование — один из самых важных методов оценки слизистой оболочки желудка. Применение дополнительных методик и техник, таких как эндоскопия в узком спектре света, эндоскопия с оптическим увеличением изображения, хромоэндоскопия, позволяют детально изучить структурные особенности слизистой оболочки желудка.
Увеличительная эндоскопия
Первое эндоскопическое исследование с применением оптического увеличения эндоскопического изображения желудка было выполнено еще в 1967 году в Японии (Okuyama) [24]. Это послужило отправной точкой для развития новых эндоскопических технологий, направленных на изучение мельчайших структур поверхности слизистой оболочки. В настоящее время существует два способа увеличения — электронное и оптическое. Изображение, полученное при помощи электронного увеличения, имеет такое же разрешение, как и обычное эндоскопическое изображение. В то время как при применении оптического увеличения становятся видимыми мельчайшие детали, которые невозможно обнаружить при обычном исследовании. Эндоскопы с увеличением оснащены
Узкоспектральная эндоскопия (narrow band imaging — NBI) — это новая оптическая диагностическая методика, которая основана на использовании специальных оптических фильтров, суживающих спектр световой волны. Обычные эндоскопические системы используют практически весь видимый световой спектр от 400 до 800 нм. Новая система использует преимущества в основном двух световых волн длиной 415 и 445 нм в диагностике сосудистых структур слизистой оболочки пищеварительного тракта, так как эти световые волны хорошо поглощаются гемоглобином. Таким образом, световые фильтры позволяют получить детальное изображение сосудистого рисунка тканей, его изменений, характерных для патологических участков воспалительного генеза, а также для предраковых заболеваний и ранних форм рака. Кроме этого, новая эндоскопическая система повышает контрастность изображения, что создает эффект виртуальной хромоскопии. С технической точки зрения применение функции узкого спектра света в желудке без оптического увеличения нецелесообразно в связи с тем, что получаемое изображение оказывается слишком темным и «шумным». Это происходит
Нормальная слизистая оболочка желудка
В желудке выделяют четыре анатомических зоны: кардия, фундальный отдел (дно желудка), тело желудка, пилорический (антральный) отдел. Поверхность слизистой оболочки всех отделов желудка выстлана однослойным призматическим железистым эпителием. Для рельефа внутренней поверхности желудка характерно наличие трех видов образований — продольных желудочных складок, желудочных полей и желудочных ямочек. Желудочные складки (plicae gastricae) образованы слизистой оболочкой и подслизистой основой. Желудочные поля (areae gastricae) представляют собой отграниченные друг от друга бороздками участки слизистой оболочки. Они имеют многоугольную форму и размер поперечника от 1 до 16 мм. Наличие полей объясняется тем, что железы желудка располагаются группами, отделенными друг от друга прослойками соединительной ткани. Поверхностно лежащие вены в этих прослойках просвечивают в виде красноватых линий, выделяя границы между полями. Желудочные ямочки (foveolae gastricae) — это углубления эпителия в собственной пластинке слизистой оболочки. Они встречаются по всей поверхности желудка. Число ямочек в желудке достигает почти трех миллионов. Желудочные ямочки имеют микроскопические размеры, но величина их неодинакова в различных отделах желудка. В кардиальном отделе и теле желудка их глубина составляет всего ¼ толщины слизистой оболочки. В пилорической части желудка ямочки более глубокие. Они занимают около половины толщины всей слизистой оболочки [27]. При обычном эндоскопическом исследовании нормальная слизистая оболочка желудка
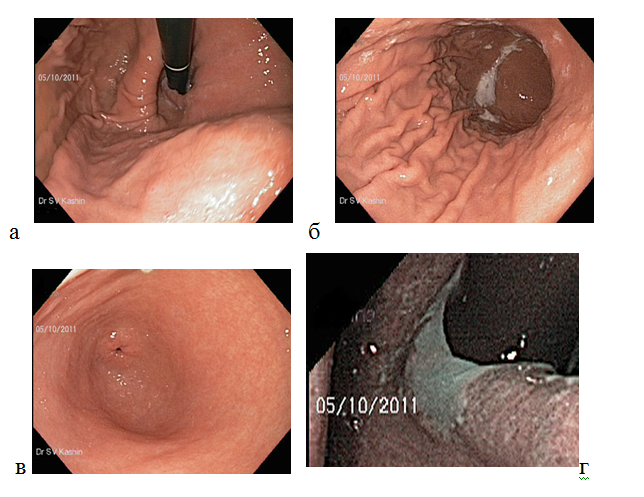
Рисунок 4. Нормальная слизистая оболочка тела желудка при стандартном осмотре в белом световом режиме. Вид тела желудка (а) при инверсии (изгибе дистального конца эндоскопа на 180о) и (б) — при прямом осмотре эндоскопом; (в) — слизистая оболочки антрального отдела желудка; (г) — осмотр в узкоспектральном режиме: более контрастное изображение поверхности слизистой оболочки кардиального и субкардиального отделов желудка, мелкозернистая структура эпителия, четкая граница с плоским эпителием пищевода (указана стрелками).
Применение узкоспектральной эндоскопии в комбинации с оптическим увеличением изображения позволяет дифференцировать патологические изменения, которые при обычной эндоскопии не могут быть выявлены. Однако следует отметить, что применение этих технологий не может полностью обеспечить различение абсолютно нормальной слизистой оболочки от гастрита с минимальными изменениями. При осмотре слизистой оболочки с увеличением оцениваются две основные характеристики — микроструктура поверхности слизистой оболочки (ямочный рисунок — pit pattern) и микрососудистая структура (рисунок субэпителиальной капиллярной сети (subepithelial capillary network — SECN). Более тридцати лет назад Sakaki предложил классификацию типов рисунка слизистой оболочки желудка при использовании фиброскопа с увеличением в 30 раз. Согласно этой классификации (рис. 5), выделяют чистые типы (А, В, С, D) и смешанные типы (АВ, ВС, CD). Типы, А и В соответствуют нормальной слизистой оболочке. Дальнейшие изменения рисунка ямок свидетельствуют о более выраженных предопухолевых изменениях, таких как атрофия и кишечная метаплазия (показаны красной и синей полосами в нижней части рисунка). Для диспластических изменений и опухолевого процесса типы рисунка могут соответствовать С (полосатый тип) и D (нерегулярный, зернистый, ячеистый рисунок) типам рисунка.
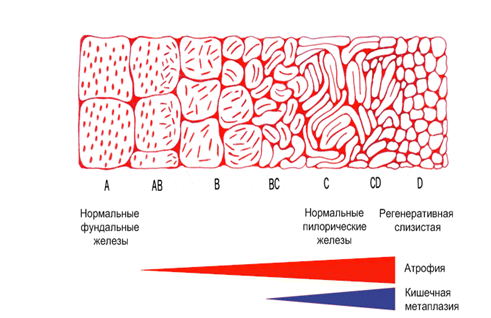
А — точечные ямки (dotted pits)
В — короткие линейные ямки (short linear pits)
С — полосатые борозды (striped grooves)
D — ячеистые борозды (
Рисунок 5. Схема классификации типов рисунка поверхности слизистой оболочки желудка при увеличительной эндоскопии (по Sakaki).
Оценивая микрососудистую архитектонику в теле желудка, можно определить рисунок субэпителиальной капиллярной сети (SECN) в виде пчелиных сот (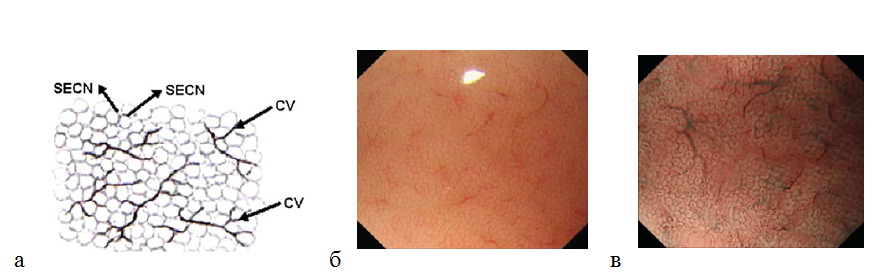
Рисунок 6. (а) — рисунок (схема) субэпителиальной капиллярной сети (SECN) в виде пчелиных сот с коллекторными венулами (CV); (б) — нормальная слизистая оболочка тела желудка: эндоскопическое изображение поверхности слизистой оболочки с увеличением изображения: субэпителиальный капиллярный рисунок в виде пчелиных сот с коллекторными венулами; (в) — эндоскопия с увеличением изображения в узкоспектральном световом режиме: более отчетливо видны желудочные ямки округлой или овальной формы, сосудистый рисунок.
Нормальная слизистая оболочка в антральном отделе
Слизистая оболочка антрального отдела желудка имеет другую картину. При исследовании микрососудистой архитектоники определяется кольцеобразная (
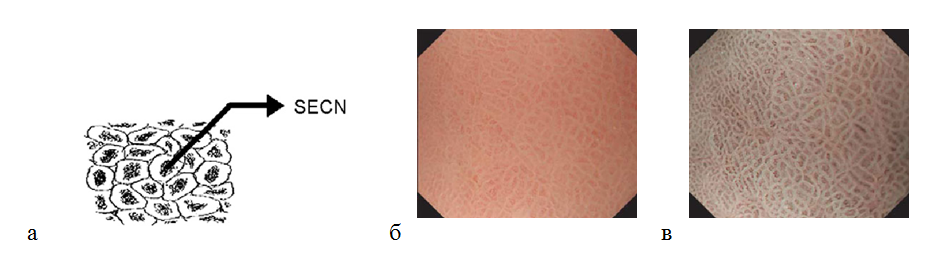
Рисунок 7. (а) — кольцеобразная субэпителиальная капиллярная сеть (SECN) в антральном отделе желудка; (б) — нормальная слизистая оболочка антрального отдела желудка: эндоскопическое изображение поверхности слизистой оболочки с увеличением изображения: кольцеобразный субэпителиальный капиллярный рисунок; (в) — эндоскопия с увеличением изображения в узкоспектральном световом режиме: более отчетливо определяется кольцеобразный субэпителиальный капиллярный рисунок и сетчатая микроструктура поверхности слизистой оболочки.
При увеличительной эндоскопии H.pylori ассоциированный гастрит с выраженными воспалительными изменениями имеет специфическую картину: микрососудистая архитектоника: в теле желудка определяется субэпителиальный капиллярный рисунок в виде пчелиных сот с правильными округлыми, овальными или тубулярными ямками, но без коллекторных венул. Возможна и другая эндоскопическая картина: расширенные белые ямки, окруженные эритемой с потерей нормального субэпителиального капиллярного рисунка и коллекторных венул. В антральном отделе определяется нерегулярный ямочный рисунок с потерей нормального субэпителиального капиллярного рисунка. При атрофических изменениях возникает утрата тонких структур слизистой оболочки (нормального субэпителиального капиллярного рисунка и округлых ямок) с нерегулярным расположением коллекторных венул и растянутых микрососудов. Определяется плоский или бесструктурный тип микроструктуры поверхности слизистой оболочки, который характеризуется отсутствием ямочного рисунка. Изменения сосудистого рисунка коррелируют со степенью атрофии слизистой оболочки [30] (рис. 8).
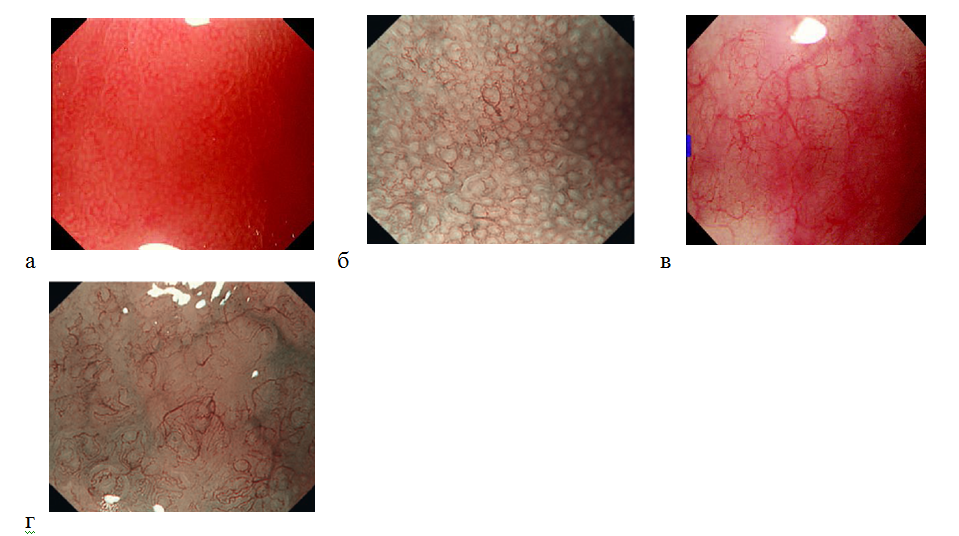
Рисунок 8. (а, б) — для H.pylori ассоциированного гастрита характерна неправильная нерегулярная микроструктура поверхности, с уменьшением выраженности капиллярной сети в отличие от нормальной слизистой оболочки с правильной регулярной микроструктурой и микрососудистой архитектоникой; эндоскопическая картина с оптическим увеличением изображения и с применением узкоспектрального режима (б) — правильный рисунок поверхности эпителия имеет вид пчелиных сот без регулярных коллекторых венул (CV), определяются округлые, овальные или тубулярные ямки правильной формы и взаиморасположения; (в, г) — при атрофическом H.pylori ассоциированном гастрите увеличительная эндоскопия в узкоспектральном режиме позволяет определить расширенные ямки (белого цвета), окруженные эритемой; при атрофии происходит утрата правильного субэпителиального капиллярного рисунка (SECN), неправильные коллекторные вены (CV), нерегулярный ямочный рисунок или отсутствие ямочного рисунка.
Кишечная метаплазия — один из главных маркеров атрофического H.pylori ассоциированного гастрита. В эндоскопической диагностике кишечной метаплазии широко используется хромоскопия с метиленовым синим. Этот краситель активно поглощается клетками тонкой и толстой кишки, окрашивая очаги кишечной метаплазии в синий цвет. При комбинированном использовании увеличительной эндоскопии и узкоспектральной эндоскопии в участках кишечной метаплазии определяются характерные гребни
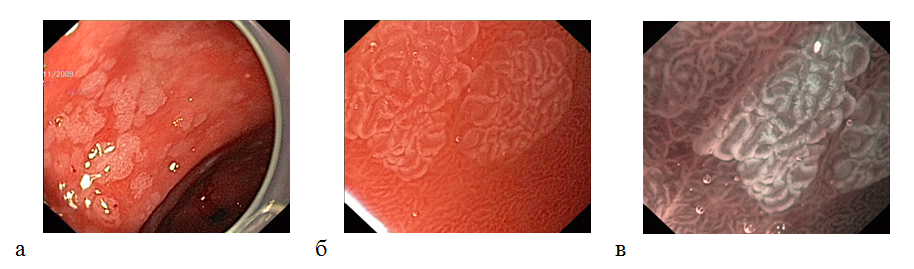
Рисунок 9. Диагностика и характеристика очагов кишечной метаплазии эпителия с помощью узкоспектральной и увеличительной (х100) эндоскопии: (а) — множественные очаги кишечной метаплазии антрального отдела желудка у пациента с H.pylori ассоциированным атрофическим гастритом; (б) — участок кишечной метаплазии при осмотре в стандартном режиме (белый свет) с оптическим
Дисплазия эпителия желудка
Согласно рекомендациям Международного комитета ВОЗ по гистологической классификации предраковых заболеваний желудка (1978), под дисплазией понимают гистологические изменения эпителия, предшествующие развитию рака. Она может наблюдаться как в
изменениями сосудистого рисунка (рис. 10).
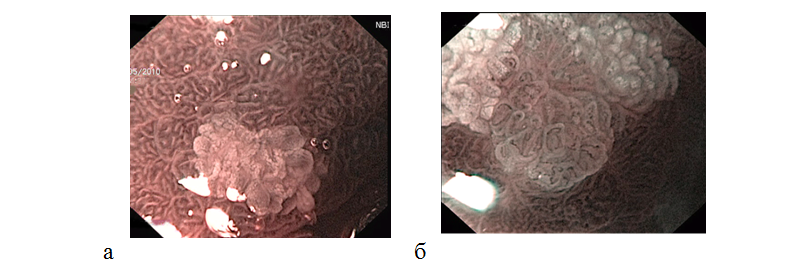
Рисунок 10. Диагностика и характеристика очагов кишечной метаплазии и дисплазии эпителия с помощью узкоспектральной и увеличительной (х100) эндоскопии: (а) — очаг кишечной метаплазии на фоне H.pylori ассоциированного гастрита; (б) — в центральной части другого участка кишечной метаплазии диагностирована зона дисплазии, для которой характерно нарушение регулярности ямок эпителия, неправильное взаиморасположение ворсинчатых структур, патологические изменения сосудистого рисунка.
Заключение
Инфекция H.pylori имеет глобальное значение и широко распространена, в том числе и в нашей стране, где по эпидемиологическим данным инфицированы более 70–80% взрослого населения. Методы диагностики инфекции H.pylori делятся на инвазивные, требующие проведения эндоскопического исследования и неинвазивные. Используемые методики могут быть прямыми, позволяющими непосредственно визуализировать возбудителя (исследование культуры, гистологическое и микроскопическое определение микроорганизма, выявление ДНК или антигена микроорганизма) или непрямыми — косвенно указывающими на возможность присутствия возбудителя в организме пациента (определение уреазной активности, определение антител). Выбор теста зависит в большой степени от его доступности и стоимости и включает различие между методами в возможности определения заболевания и использования результатов для подтверждения эрадикации.
Согласно новым европейским рекомендациям (Маастрихт 4), одним из условий достоверности применяемых методов диагностики инфекции H.pylori, включающей использование бактериологического, гистологического методов, быстрого уреазного и дыхательного тестов, а также определения ДНК или антигена бактерий в кале, является прекращение приема ингибиторов протонной помпы как минимум за две недели перед тестированием. Если это невозможно, может быть проведена серологическая диагностика. H.pylori практически у всех инфицированных индивидуумов вызывает воспалительные изменения в гастродуоденальной слизистой оболочке, которые и представляют собой собственно субстрат гастрита. H.pylori ассоциированный гастрит — наиболее распространенный вариант гастрита. Другие особые формы гастрита составляют не более 10%, среди которых 5% — аутоиммунный гастрит. Таким образом, воспаление слизистой оболочки желудка, вызванное H.pylori, составляет 90% среди всех форм гастритов. Хронический гастрит рассматривается как одно из важных звеньев в цепи процессов, приводящих к развитию предраковых изменений слизистой оболочки и в конечном итоге к аденокарциноме желудка. Своевременная диагностика и лечение этих патологических процессов крайне важны для определения методов их своевременного лечения.
Литература
Аруин Л. И., Григорьев П. Я., Исаков В. А., Яковенко
Анкудинова С. А., Заречнова Н. Н., Кибарова
Ивашкин
Steer H. Ultrastructure of cell migration through the gastric epithelium and its relationship to bacteria. J Clin Pathol 1975; 28: 639–646.
Marshall B. Unidentified curved bacilli on gastric epithelium in active chronic gastritis. Lancet 1983; 1: 12731–12734.
Goodwin CS, Armstrong JA, Chilvers T, et al. Transfer of Campylobacter pylori and Campylobacter mustelae to Helicobacter gen. nov. as Helicobacter pylori comb. nov. and Helicobacter mustelae comb. nov. respectively. Int J Syst Evol Microbiol 1989; 39: 397–405.
Forman D. Helicobacter pylori: the gastric cancer problem. Gut. 1998 July; 43(Suppl 1):
IARC. Working Group. IARC Monographs on the Evaluation of Carcinogenic Risk to Humans. Schistosomes, liver flukes and Helicobacter Pylori, Vol. 61. Lyon, France: IARC, 1994.
Щербаков
Kikuchi S. Epidemiology of Helicobacter pylori and gastric cancer. Gastric Cancer. 2002; 5 (1): 6–15.
Uemura N., Okamoto S., Yamamoto S., et al. Helicobacter pylori Infection and the Development of Gastric Cancer. N Engl J Med 2001; 345: 784–789.
Heilmann KL, Borchard F. Gastritis due to spiral shaped bacteria other than Helicobacter pylori: Clinical, histological and ultrastructural findings. Gut 1991; 32: 137–40.
Rugge M, Meggio A, Pennelli G, et al. Gastritis staging in clinical practice: the OLGA staging system. Gut 2007; 56: 631–636.
Rugge M, Correa P, Di Mario F,
Пасечников В. Д., Чуков С. З., Бакланова
Аруин Л. И., Кононов А. В., Мозговой
Пасечников В. Д., Чуков
Маев И. В., Мельникова Е. В., Крюкова Т. В., Кашин С. В., Надежин
Tomb J, White O, Kerlavage A et al. (1997). The complete genome sequence of the gastric pathogen Helicobacter pylori. Nature 388 (6642): 539–47.
Момыналиев
Blaser MJ. Intrastrain differences in Helicobacter pylori: a key question in mucosal damage? Ann Med. 1995 Oct; 27 (5): 559–563.
Atherton JC. The clinical relevance of strain types of Helicobacter pylori. Gut. 1997 Jun; 40 (6): 701–703.
Mobley HL. Defining Helicobacter pylori as a pathogen: strain heterogeneity and virulence. Am J Med. 1996 May 20; 100 (5A):
Okuyama Y, Takemoto T, Tsuneoka K et al. Specially designed gastroscope for magnified observation. Gastroenterol. Endosc. 1967; 9: 42–3 (in Japanese).
Comprehensive Atlas of High Resolution Endoscopy and Narrowband Imaging/ edited by Jonathan Cohen. — 1st ed. — Oxford; Massachusetts; Victoria.: Blackwell Publishing, 2007. — 318 p.
Гистология: учебник
Терминология определения терминов и диагностические критерии в эндоскопии пищеварительного тракта: эндоскопия пищеварительного тракта: номенклатура OMED/ Зденек Маржатка. При сотрудничестве комитета по терминологии OMED. Введ.:
Bansal A., Ulusarac O., Mathur S., Sharma P. Correlation between narrow band imaging and nonneoplastic.gastric pathology: a pilot feasibility trial. GASTROINTESTINAL ENDOSCOPY, Vol 67, No. 2: 2008, p. 210–216.
George C.

